|
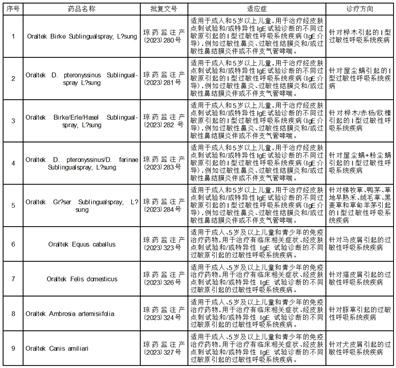
本公司董事会及全体董事保证本公告内容不存在任何虚假记载、误导性陈述或者重大遗漏,并对其内容的真实性、准确性和完整性依法承担法律责任。 重要内容提示: ● 江苏浩欧博生物医药股份有限公司(以下简称“浩欧博”或“公司”)基于战略规划,与Inmunotek S.L.,公司(以下简称:Inmunotek公司)签订独家排他战略合作协议,由公司独家将Inmunotek公司旗下Oraltek^[R](欧脱克^[R])(以下简称“欧脱克”)系列脱敏药品引进中国市场,开展欧脱克系列脱敏药品的国内销售和注册,以实施公司在国内脱敏药领域新业务,打通过敏行业上下游业务,有助于解决因没有相关药物治疗严重影响过敏诊疗行业发展、制约过敏检测业务发展的问题,满足过敏患者的诊疗需求。 ● 公司于2023年9月5日召开了第三届董事会第三次会议以及第三届监事会第三次会议,审议通过了《关于公司开展新业务的议案》。根据《江苏浩欧博生物医药股份有限公司章程》以及《上海证券交易所科创板股票上市规则》的规定,本次对新业务的投资无需提交股东大会审议。 ● 新业务的实施计划和投资金额: 项目一期投资约3,500万人民币,主要用于欧脱克系列产品在海南自由贸易港博鳌乐城国际医疗旅游先行区(以下简称“乐城先行区”)医院的销售、产品采购、建立库存及培训和宣传等方面。 项目二期将依托欧脱克在乐城先行区开展的真实世界研究,开展欧脱克产品在中国的注册。 公司将以自有资金开展上述新业务,并根据真实世界研究的情况,审慎开展项目二期投资。 ● 相关风险提示: 1、先期欧脱克系列产品仅可在乐城先行区医院销售,能否成功推荐患者到乐城使用尚需公司实际开展宣传推广工作,同时按国家现行相关法规,患者必须亲自到乐城接受诊疗、支付相关诊疗费用,目前每次只能开具3个月使用的药品。因此欧脱克系列产品的推广销售存在不及预期的风险。 2、公司是国内提供过敏检测产品和服务的专业公司,每年为百万级患者提供过敏检测服务。虽然新业务与浩欧博的过敏检测业务有较强的协同性,但浩欧博迄今没有药品推广销售的经验,团队建设和经验积累也需要时间。 3、后续公司将以欧脱克系列产品在乐城先行区开展的真实世界研究为基础,进行欧脱克系列产品在国内的药品注册,但存在不予注册的风险,同时浩欧博迄今尚没有国内药品注册的经验,虽然不开展真实世界研究和国内注册并不影响产品在乐城先行区的销售,但会对产品在国内广大地区的销售产生影响。 一、新业务投资概述 浩欧博基于战略规划,结合市场发展前景和业务布局,以自有资金开展欧脱克系列脱敏药品的销售和注册业务,首期投资额约3,500万人民币,主要用于欧脱克系列产品在乐城先行区医院的销售、产品采购、建立库存及培训和宣传等方面,后期开展欧脱克产品在中国的注册工作。本次投资的资金来源于自有资金,本次交易不构成关联交易,亦不构成重大资产重组。 公司前期已经与Inmunotek公司签订独家排他战略合作协议,由公司独家将欧脱克系列产品引进中国市场。近期双方已进一步签订协议,明确双方的独家战略合作包括乐城先行区申请特批使用、在中国的进口药品注册、以及完成进口药品注册后的全国销售。根据协议,浩欧博全权负责欧脱克系列产品在中国的定价和销售,协议期限25年并在期满后可以自动续签。 公司已于2023年9月5日召开了第三届董事会第三次会议以及第三届监事会第三次会议,审议通过了《关于公司开展新业务的议案》。根据《江苏浩欧博生物医药股份有限公司章程》以及《上海证券交易所科创板股票上市规则》的规定,本次投资无需提交股东大会审议。 二、新业务基本情况 1、新业务的政策背景 乐城先行区是全国唯一的“医疗特区”,位于海南省琼海市博鳌镇,临近博鳌亚洲论坛核心区。2013年2月28日,国务院批复同意设立乐城先行区,并赋予九项独一无二的支持政策,可概括为“四个特许”:特许医疗、特许研究、特许经营和特许国际交流。 2018年12月,国务院印发《关于在海南博鳌乐城国际医疗旅游先行区暂时调整实施〈中华人民共和国药品管理法实施条例〉有关规定的决定》,规定对先行区内医疗机构因临床急需进口药品(不含疫苗)的申请,由海南省人民政府实施审批。 2019年9月,国家发展改革委、国家卫生健康委、国家中医药局、国家药监局印发《关于支持建设博鳌乐城国际医疗旅游先行区的实施方案》,被称为新“国九条”,提出要对标国际最高标准,以高水平开放推动国际医疗旅游和高端医疗服务发展,打造海南国际旅游消费中心建设的重要支撑平台,到2025年实现医疗技术、装备、药品与国际先进水平“三同步”。 2021年9月,海南省药监局、海南省卫生健康委、海口海关联合印发《进一步优化监管服务支持海南博鳌乐城国际医疗旅游先行区高质量发展若干措施》,进一步优化临床急需进口药品医疗器械的审批流程、审批模式等,便利公众及时使用临床急需进口药品医疗器械。 乐城先行区允许在国外已经获批上市但在国内尚未批准的药品,在乐城先行区使用。目前患者可以在乐城先行区的医院就诊并允许携带三个月用量的药品离岛,随着相关试点政策的不断推进,预计未来将持续优化带药离院管理办法。 同时,乐城先行区作为我国首个开展临床真实世界应用试点的区域,可利用特许药械政策,开展临床真实世界数据应用试点工作,探索将未经中国注册、经批准在乐城先行区使用的特许药械临床数据转化为真实世界证据,加快进口药械的注册审批速度。据人民日报2023年8月1日报道:自2020年3月26日首个产品获批以来,已有10个试点产品(3个药品、7个医疗器械)利用乐城真实世界证据辅助临床评价获得国内注册,其中半数产品均在申报注册半年内获得批准。 2、欧脱克系列产品情况 欧脱克产品系列是Inmunotek公司生产的舌下喷剂脱敏产品。共有12种产品涵盖17种过敏原,包括屋尘螨、粉尘螨、桦树花粉、艾蒿、普通豚草、猫皮屑、狗皮屑、马皮屑、链格孢霉(常见霉菌的一种)、梯牧草花粉、鸭茅草花粉、草地早熟禾花粉、绒毛草花粉、黑麦草花粉、草甸羊毛草花粉、杨树花粉、欧榛树花粉。 Inmunotek公司由免疫学家Jose Luis Subiza博士于1992年在西班牙著名的过敏学家和孢粉学先驱Eliseo Subiza的临床实验室的基础上创立,其拥有多种脱敏药物产品组合。Inmunotek公司被CEPYME500、FT1000、Inc5000等欧洲和全球主要排名机构列入欧洲快速增长的高科技公司。Inmunotek公司被西班牙科学和创新部授予国家创新奖,这是西班牙在创新领域最重要的奖项。 欧脱克产品系列基本上覆盖了主要的吸入性过敏原,可基本满足吸入性过敏原脱敏治疗的临床需求。欧脱克系列产品已在全球十几个国家长期销售,其安全性和有效性得到了验证。欧脱克产品系列与浩欧博的过敏检测业务有较强的协同性,可以为医疗机构和广大患者提供过敏诊疗全面解决方案。 近期,由瑞金海南医院、海南超级医院提出申请的欧脱克12个产品,获得海南省药监局获批准,具体明细如下: 3、新业务的行业情况 脱敏治疗是过敏性疾病对因治疗方式。国内目前主要开展粉尘螨脱敏治疗,但除了螨过敏原以外,常见的吸入性过敏原还有动物皮毛(尤其猫毛、狗毛)、草花粉、树花粉、霉菌等,多数患者也表现为多重过敏,即对多个过敏原阳性,多种过敏原联合治疗,更能满足临床需求。但国内的过敏原脱敏治疗产品种类少,长期无法满足临床需求。 目前,国内仅有浙江我武生物科技股份有限公司(股票代码:300357)具有“粉尘螨”和“黄花蒿”两种过敏原的脱敏治疗舌下滴剂。另有,丹麦爱尔开-阿贝优公司以及阿罗格(北京)医药科技有限公司的螨脱敏的针剂,获得中国的注册证,在国内销售。 公司独家将欧脱克产品引进中国市场,可以促进公司在过敏检测产品和服务方面的销售,并与公司正在开展的线上线下结合的过敏疾病诊疗实现协同效应,进一步巩固公司在过敏检测领域的优势地位,为中国的广大过敏患者提供更好的诊疗产品和服务。 4、新业务的商业模式 按照法律法规规定,公司已设立全资子公司浩欧博(新加坡)有限公司,并与具有药品进口批发资质的乐城先行区进口批发企业合作,由浩欧博(新加坡)有限公司采购欧脱克产品系列,通过合作的进口批发企业供应乐城先行区的医疗机构。同时,公司将向现有检测客户、用户以及广大患者推广和介绍欧脱克产品系列,推荐乐城先行区的治疗服务。 5、新业务的管理情况 公司全资子公司浩欧博(新加坡)有限公司将负责现阶段产品采购和销售业务,纳入公司合并报表范围内,公司将在以下方面强化日常管理: (1)经营管理方面:公司将在临床研究、业务渠道、产业整合等方面进行统筹规划,充分发挥公司业务之间的协同效应,实现各业务之间的优势互补,拓宽公司产品的市场领域,最终实现公司产品战略的落地,促进公司长远发展。 (2)财务管理方面:实施本项目的事业部和控股子公司财务由公司实行全面管理。 (3)在组织架构方面:公司将聘任具有相关经验以及专业管理能力的核心人员对事业部和子公司进行专业化运营及管理。 6、新业务审批情况 目前,本次新业务开展的Oraltek^[R](欧脱克^[R])系列产品包括12个产品(覆盖17种吸入性过敏原)由瑞金海南医院、海南超级医院提出申请,并已全部获得海南省卫健委和海南省药监局批准及在乐城先行区使用。 三、开展新业务的合理性和必要性分析 1、开展新业务的原因 (1)新业务有庞大明确的市场需求 中国国内有4亿过敏患者,过敏原检测已经在国内广泛开展,目前国内大多数三级医院均已开展过敏检测,以浩欧博为代表的国内企业已能够提供50种以上的过敏原检测产品,覆盖临床所需的主要食物和吸入性过敏原。但受制于各种因素,脱敏治疗产品种类少,患者接受程度不高。随着过敏疾病被越来越多的医患了解、接受,随着过敏诊疗事业的不断发展,脱敏治疗作为唯一的对因性治疗手段将被越来越多的医生和患者接受。据浙江我武生物科技股份有限公司2022年年报披露,我国脱敏治疗市场规模持续扩大,2022年其实现营业收入8.96亿元,其中粉尘螨滴剂贡献8.79亿元,在经济环境影响之下,仍然增长10.44%。国内目前仅有螨和黄花蒿脱敏治疗药物,而吸入性过敏原还有猫毛、狗毛、多种树花粉、草花粉、霉菌等,这些过敏原国内尚无脱敏治疗药物。国际杂志Allergy研究表明,90%以上的过敏性鼻炎和哮喘患者,对超过一种过敏原阳性。对尘螨过敏的患者同时可能也对其他过敏原阳性,所以多过敏原联合治疗疗效更好,脱敏治疗将有巨大明确的市场需求。 (2)本项目是公司立足于自身优势,实现上下游产业结合的迫切需求 引进脱敏药项目,是公司重要的战略决策。脱敏治疗市场进入壁垒高,药品从开展临床研究到最终取得注册证书,需要较长的时间和较大的投入。从2006年我武生物的粉尘螨脱敏治疗产品“畅迪”上市迄今,国内仅有黄花蒿脱敏治疗产品上市。乐城先行区作为我国首个开展临床真实世界应用试点的区域,可利用特许药械政策,开展临床真实世界数据应用试点工作,加快进口药械的注册审批速度。开展脱敏治疗有利于加强公司在过敏诊疗领域的优势地位,有利于创造新的业务增长点,有利于增强公司的整体竞争实力,提高公司的成长性和盈利能力。 (3)本项目与公司主营业务有较强的协同效应 公司进入脱敏药领域,和公司的过敏检测业务,以及正在开展的线上线下结合的过敏疾病诊疗,有明显的协同效应和相互促进的作用。脱敏治疗必须首先确定患者对何种过敏原阳性,准确的过敏检测是脱敏治疗的前提,精确的过敏原检测结果可以有力地促进多种过敏原的脱敏治疗,而多过敏原的脱敏治疗可以有效解决“查了无法治,检查无意义”的问题,促进过敏检测业务的发展。从而能够为中国的广大过敏患者提供更好的诊疗产品和服务。 (4)本项目的实施为国内过敏学科发展、临床研究提供更多可能性 公司与过敏领域具有几十年丰富经验的Inmunotek公司战略合作,共同开展临床研究和技术合作,有助于提高公司在过敏诊疗领域的专业化、国际化水平。 本项目有望改变国内脱敏治疗产品少的状况,为医生提供更多的治疗手段,为患者提供更多的治愈结果,为临床研究提供更多的可能性,促进学科发展,造福广大患者。 2、公司的准备情况 公司就新业务的可行性进行了论证,在人才储备、市场拓展、资金安排等方面均有所布局和筹划,新业务可以充分利用公司现有的技术、产品和管理的资源优势,实现快速布局。新加坡子公司设立后将加快相关专业人员的引进,进一步扩大团队规模。 经过公司的前期准备,目前Oraltek^[R](欧脱克^[R])系列产品包括12个产品(覆盖17种吸入性过敏原)已获得海南省卫健委和海南省药监局批准及在乐城先行区使用。 四、新业务对公司的影响 1、对公司生产经营的影响 本次投资开展新业务是公司为实现公司战略目标、立足长远利益作出的慎重决策,有利于进一步拓展公司的产品种类,实现上下游产业结合,延伸公司的产业链布局,是实现公司长期可持续盈利目标的重要战略。 2、对公司的财务状况和经营成果影响 本次开展新业务是公司战略发展的需要,使用公司自有资金,不会对公司目前的财务和经营状况产生重大不利影响,不存在损害公司、公司股东,特别是中小股东利益的情形。 3、本次开展新业务不存在关联交易和同业竞争的事项。 五、风险提示 1、先期欧脱克系列产品仅可在乐城先行区医院销售,能否成功推荐患者到乐城使用尚需公司实际开展宣传推广工作,同时按国家现行相关法规,患者必须亲自到乐城接受诊疗、支付相关诊疗费用,目前每次只能开具3个月使用的药品。因此欧脱克系列产品的推广销售存在不及预期的风险。 2、公司是国内提供过敏检测产品和服务的专业公司,每年为百万级患者提供过敏检测服务。虽然新业务与浩欧博的过敏检测业务有较强的协同性,但浩欧博迄今没有药品推广销售的经验,团队建设和经验积累也需要时间。 3、后续公司将以欧脱克系列产品在乐城先行区开展的真实世界研究为基础,进行欧脱克系列产品在国内的药品注册,但存在不予注册的风险,同时浩欧博迄今尚没有国内药品注册的经验,虽然不开展真实世界研究和国内注册并不影响产品在乐城先行区的销售,但会对产品在国内广大地区的销售产生影响。 综上,脱敏治疗、进口药品代理销售、进口药品基于真实世界研究的国内注册,对于公司都是全新的业务。过敏诊疗患者能否接受治疗,药品进口环节较多,真实世界研究是否获得成功进而能否取得国内注册并在全国使用等均存在不确定因素的影响,公司存在新业务拓展不及预期的风险,上述业务对公司未来业绩的影响具有不确定性。公司将密切关注新业务后续进展,积极防范和应对项目实施过程中可能面临的各种风险,并严格按照相关法律、法规及规范性文件的要求,及时履行信息披露义务。敬请广大投资者谨慎投资,注意投资风险。 特此公告。 江苏浩欧博生物医药股份有限公司 董事会 二〇二三年九月六日
|